|
КУРС : "Физическая химия"
|
|
Информация о подразделении, отвечающего за СЭУМК.
| Подразделение разработчик СЭУМК |
Разработчики СЭУМК |
|
Кафедра физической и аналитической химии
Институт природных ресурсов
|
Сметанина Евгения Ильинична, к.т.н., доцент
|
Список дисциплин использующих СЭУМК "Физическая химия" в учебном процессе.
|
|
Обеспечивающая кафедра
|
Код специальности, специальность
|
№, Дисциплина
|
Уровень
|
Курс
|
Форма обучения
|
Количество часов, (Аудиторная, Самостоятельная, Кредиты)
|
Форма контроля
|
| ФАХ |
18.03.01
Химическая технология
|
МЕЦ.Б.5.0
Физическая химия
|
бакалавр |
2 |
очная |
198(96/102)
8 кредитов
|
экзамен |
| ФАХ |
18.03.02
Энерго- и ресурсосберегающие процессы в химической технологии, нефтехимии и биотехнологии
|
МЕЦ.Б.5.0
Физическая химия
|
бакалавр |
2 |
очная |
198(96/102)
8 кредитов
|
экзамен |
|
| ЦЕЛИ КУРСА |
|
Формирование:
- способности понимать физико-химическую сущность процессов и использовать основные законы физической химии в комплексной производственно-технологической деятельности
- способности выполнять расчеты физико-химических параметров химических процессов на основе методов физической химии
- творческого мышления, объединение фундаментальных знаний основных законов и методов проведения физико-химических исследований, с последующей обработкой и анализом результатов исследований
- навыков самостоятельного проведения теоретических и экспериментальных физико-химических исследований
|
|
МЕЖПРЕДМЕТНЫЕ СВЯЗИ
|
|
Согласно ФГОС и ООП «Химическая технология» дисциплина «Физическая химия» является базовой дисциплиной и относится к естественнонаучному циклу. До освоения дисциплины «Физическая химия» должны быть изучены следующие дисциплины (пререквизиты): математика, физика, химия.
Кроме того, для успешного освоения дисциплины «Физическая химия» параллельно должны изучаться дисциплины (кореквизиты): органическая химия, аналитическая химия и физико-химические методы анализа
|
|
СТРУКТУРА ТЕОРЕТИЧЕСКОЙ ЧАСТИ КУРСА
|
|
1.Законы термодинамики
2. Термодинамические потенциалы
3. Химическое равновесие
4. Фазовое равновесие
5. Растворы
|
|
СТРУКТУРА ПРАКТИЧЕСКОЙ ЧАСТИ КУРСА
|
|
Практические занятия:
1. Расчет тепловых эффектов химических реакций.
2. Расчеты, связанные с определением теплоемкости и количества теплоты.
3. Зависимость теплового эффекта химической реакции от температуры (закон Кирхгофа).
4. Расчет изменения энтропии в различных процессах.
5. Расчет термодинамических потенциалов в различных процессах.
6. Вычисление константы равновесия и степени диссоциации.
7. Расчет равновесного состава смеси.
8. Определение направления процесса по уравнению изотермы химической реакции.
9. Зависимость константы равновесия от температуры.
10. Расчет фазового равновесия в однокомпонентных системах.
11. Анализ фазовых диаграмм состояния двухкомпонентных систем.
12. Расчет состава растворов.
13. Вычисление парциальных молярных величин.
14. Законы предельно разбавленных растворов.
Лабораторные работы:
1. Определение теплоты растворения неизвестной соли.
2. Определение теплоты парообразования легколетучих жидкостей.
3. Исследование химического равновесия в гетерогенной системе.
4. Термический анализ. Построение диаграммы плавкости системы дифениламин-нафталин.
5. Перегонка бинарных смесей.
6. Определение молекулярного веса вещества методом криоскопии.
|
| КЛЮЧЕВЫЕ СЛОВА |
|
термодинамическая система, термодинамические параметры, компонент, фаза, химический потенциал, константа равновесия, парциальные молярные величины, термодинамическая теория растворов, типы растворов и их свойства
|
| ИНФОРМАЦИЯ ДЛЯ СВЯЗИ С ПРЕПОДАВАТЕЛЯМИ |
|
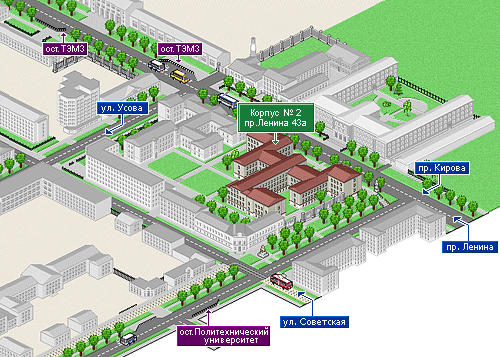
г. Томск, проспект Ленина, 43/A,
Учебный корпус №2, офис 236
Сметанина Евгения Ильинична, к.т.н., доцент кафедры ФАХ ИПР ТПУ, тел. 563-860, eis@tpu.ru
Copyright ©2014. Tomsk Polytechnic University,
All rights reserved.
|
